1995. évi XCII. törvény
a takarmányok előállításáról és forgalomba hozataláról1A végrehajtásáról szóló 25/1996. (IX. 4.) FM rendelettel egységes szerkezetben.
[A vastag betűs szedés az 1995. évi XCII. törvény (Tv)., a normál betűs szedés a 25/1996. (IX. 4.) FM rendelet (Vhr.) szövege.]
Az Országgyűlés annak érdekében, hogy a takarmányok biztosítsák az állatok korcsoportjának és hasznosítási irányának megfelelő táplálóanyag-tartalmat, és a gazdasági haszonállatok esetében szolgálják a genetikai potenciál hatékony kihasználását, valamint ne károsítsák az állatok egészségét és megfeleljenek az állattartás állatvédelmi előírásainak, továbbá, hogy az állati eredetű termékek megfeleljenek az előírt minőségi követelményeknek, tekintettel az emberi egészségre való ártalmatlanságukra, valamint, hogy védje a takarmány-felhasználók érdekeit, a takarmányok előállításának, forgalomba hozatalának és felhasználásának feltételeiről a következő törvényt alkotja:
A takarmányok előállításáról és forgalomba hozataláról szóló 1995. évi XCII. törvény ( a továbbiakban: Tv.) 20. §-ában kapott felhatalmazás alapján – az érdekelt miniszterekkel egyetértésben – a következőket rendelem el:
Bevezető rendelkezések
Tv.1. § (1) E törvény hatálya kiterjed
a) a takarmányok, takarmány-alapanyagok, takarmány-kiegészítőanyagok, takarmány-adalékanyagok, gyógyszeres takarmányok, előkeverékek, takarmánykeverékek, tápok, tápszerek előállítására, importjára, forgalomba hozatalára, forgalmazására, felhasználására, minőségvizsgálatára és -ellenőrzésére;
b) a takarmányok előállításával, importálásával, forgalomba hozatalával, forgalmazásával és felhasználásával foglalkozó valamennyi természetes és jogi személyre, valamint jogi személyiséggel nem rendelkező gazdasági társaságra.
(2) A törvény rendelkezéseit megfelelően alkalmazni kell a forgalomba hozott és az importált szálas- és tömegtakarmányok esetében is.
Tv.2. § E törvény alkalmazása szempontjából
1. takarmány: az állatok táplálására, etetésére szolgáló növényi vagy állati termék természetes állapotban, frissen vagy tartósítva, valamint ezek iparilag feldolgozott készítményei, melléktermékei, továbbá szerves és szervetlen anyag, önmagában vagy keverék formájában, adalékanyagokkal vagy azok nélkül;
2. takarmány-alapanyag: azok a természetes eredetű vagy mesterséges folyamatok eredményeként keletkező növényi, állati, ásványi vagy szintetikus, fermentációs, illetve egyéb technológiával előállított takarmányok, amelyek meghatározott arányú összekeverésével előkeveréket, takarmánykeveréket, tápot és tápszert lehet előállítani;
3. takarmány-kiegészítőanyag: olyan anyag, amely növeli a takarmány tápértékét, élettani hatását, és nem tartozik az állatgyógyászati készítményekre vonatkozó szabályok hatálya alá;
4. nem nutritív testidegen takarmány-kiegészítőanyag: tápláló értékkel nem rendelkező, maradék képző anyag — a hozamfokozókat is ideértve — az állati testnek nem természetes alkotója, amely a takarmánykihasználás fokozására szolgál;
5. takarmány-adalékanyag: olyan anyag, amely a takarmány tulajdonságait kedvezően befolyásolja, különös tekintettel a takarmány külső megjelenésére, szagára, ízére, állományára és eltarthatóságára;
6. gyógyszeres takarmány: olyan takarmány, amely az állatgyógyászati készítményekre vonatkozó szabályok hatálya alá tartozó anyagot is tartalmaz;
7. előkeverék: különböző takarmány-alapanyagok, takarmány-kiegészítőanyagok és takarmány-adalékanyagok olyan keveréke, amely a teljes értékű takarmánykeverék gyártásához alapanyagul szolgál;
8. takarmánykeverék: állatok etetésére vagy további feldolgozás céljára a takarmány-alapanyagok összekeverésével előállított nem teljes értékű, önállóan etethető takarmány;
9. táp: teljes értékű takarmánykeverék, amely a meghatározott fajú, korú és hasznosítási irányú állat táplálóanyag szükségletét önmagában etetve kielégíti;
10. tápszer: olyan takarmány, amely anyatej helyettesítésére szolgál, és önmagában etetve alkalmas fiatal állatok felnevelésére;
11. szálas- és tömegtakarmány: természetes állapotú friss vagy tartósított kis energiatartalmú, többségében sok nyersrostot tartalmazó takarmány;
12. a takarmány nem kívánatos, mérgező anyagai: azok az anyagok, amelyek nem az állat táplálóanyag szükségletének kielégítését szolgálják, és jelenlétük az állat egészségét, termelőképességét, illetve az állati eredetű élelmiszereket fogyasztó ember egészségét veszélyeztetheti;
13. takarmány-előállítás: takarmányok előkészítése, feldolgozása, keverése és kiszerelése;
14. új takarmány: engedély vagy szabvány nélkül, a korábbitól eltérő eljárással készült, vagy eltérő módon felhasználható, illetve új takarmányozás-élettani hatással rendelkező takarmány;
15. takarmánykezelés: a takarmány mérése, ki- és betöltése, csomagolása, hőkezelése, hűtése, tárolása, megőrzése, valamint egyéb kezelése, és minden olyan ezekhez kapcsolódó tevékenység, amely nem minősül előállításnak vagy forgalomba hozatalnak;
16. takarmányforgalmazás: a takarmányok értékesítés előtti tárolása és értékesítése;
17. takarmányelőállító üzem: az az üzem, amely takarmány-alapanyagot, takarmány-kiegészítőanyagot, takarmány-adalékanyagot, előkeveréket, vagy ezekből takarmánykeveréket, tápot, tápszert, gyógyszeres takarmányt, illetve nem nutritív testidegen takarmány-kiegészítőanyagot állít elő;
18. takarmányhigiénia: a takarmány előállításának, tárolásának, forgalomba hozatalának az állatbetegségekkel és az állategészségügyi szempontból való fogyaszthatósággal összefüggő követelményrendszere, a takarmánnyal terjeszthető fertőzés, takarmányártalom, továbbá a termék révén az emberi megbetegedés megelőzése és elhárítása;
19. takarmányellenőrzés: a takarmány előállításának, importálásának, tárolásának, forgalmazásának, felhasználásának, előzetesen megállapított tulajdonságainak, valamint a nem kívánatos, mérgező anyagoktól való mentességének és a takarmány higiéniai állapotának ellenőrzése.
(A Tv. 2. §-ához)
A takarmány előállításának, forgalomba hozatalának
és felhasználásának feltételei
Tv.3. § (1) A takarmány, a takarmány-alapanyag, a takarmány-kiegészítőanyag, a takarmány-adalékanyag, a gyógyszeres takarmány, az előkeverék, a takarmánykeverék, a táp, a tápszer és a szálas- és tömegtakarmány előállításával, forgalmazásával, forgalomba hozatalával kapcsolatos minősítési, engedélyezési, nyilvántartási és ellenőrzési feladatokat takarmányozási hatósági jogkörben a mezőgazdasági minősítő feladatokat ellátó intézet (a továbbiakban: minősítő intézet), valamint a megyei (fővárosi) állategészségügyi és élelmiszer-ellenőrző állomás (a továbbiakban: Állomás) (a minősítő intézet és az Állomás a továbbiakban együtt: takarmányozási hatóság) látja el, a törvényben meghatározott esetekben az állatgyógyászati oltóanyag, gyógyszer- és takarmányvizsgáló feladatokat ellátó intézet, mint országos hatáskörű szakértői intézmény (a továbbiakban: szakértő intézet) véleménye alapján.
(2) A törvényben meghatározott esetekben takarmányozási hatósági feladatokat lát el a Földművelésügyi Minisztérium (a továbbiakban: minisztérium) és a takarmányfelügyelő is.
(A Tv. 3. §-ához)
A takarmányelőállító üzem létesítése
Tv.4. § (1) A takarmányelőállító üzem létesítésének engedélyezéséhez az Állomás szakhatósági hozzájárulása is szükséges.
(2) A környezetvédelmi és közegészségügyi feltételek biztosítása az új takarmányelőállító üzem létesítésének előfeltétele. A takarmányelőállító üzemek létesítéséhez az illetékes környezetvédelmi felügyelőség és az Állami Népegészségügyi és Tisztiorvosi Szolgálat (a továbbiakban: ÁNTSZ) szakhatósági állásfoglalását is be kell szerezni.
(3) A takarmányelőállító üzem működésének megkezdése előtt legalább 30 nappal engedélyt kell kérni az Állomástól a takarmányelőállítási tevékenység megkezdésére és az előállítani kívánt takarmányok körére. A takarmányelőállító üzem működését az ÁNTSZ-szel és az illetékes szakhatóságokkal egyetértésben kell engedélyezni.
(4) Az engedélyben feltüntetett takarmányok körét csak az Állomás hozzájárulásával lehet bővíteni.
(5) Az Állomás legalább ötévenként felülvizsgálja, hogy a takarmányelőállító üzem megfelel-e az (1) bekezdésben foglalt feltételeknek.
(A Tv. 4. §-ához)
A takarmányelőállítás és forgalomba hozatal
Tv.5. § (1) Takarmány előállításához csak engedélyezett takarmány-alapanyagot, takarmány-kiegészítőanyagot, takarmány-adalékanyagot lehet felhasználni. Nincs szükség engedélyre a természetes állapotú, növényi eredetű, illetve szabvánnyal rendelkező alapanyagok esetében.
(2) Takarmány előállításának további feltétele:
a) a takarmány minőségi követelményeinek megfelelő előállításra alkalmas, a 4. § szerinti takarmányelőállító üzem és berendezés, valamint
b) a tevékenység folytatásához előírt szakképzettség.
(3) Takarmányt csak nyilvántartásba vett gyártmánylap alapján lehet forgalomba hozni.
(4) Tilos takarmányt, takarmány-alapanyagot, takarmány-kiegészítőanyagot, takarmány-adalékanyagot, gyógyszeres takarmányt, előkeveréket, takarmánykeveréket, tápot és tápszert, továbbá szálas- és tömegtakarmányt úgy előállítani, kezelni, forgalomba hozni, valamint felhasználni, hogy
a) a termék minősége károsan megváltozzon;
b) az állat, illetve közvetve az ember egészségét veszélyeztesse;
c) az állat termelőképességét károsan befolyásolja;
d) az a minőségében károsult takarmányok hibáit elfedje.
(5) A minőségében károsult takarmányok felhasználhatóságáról a takarmányozási hatóság dönt.
(A Tv. 5. §-ához)
A takarmány minősítése
Tv.6. § (1) A forgalomba hozatalt, illetve a felhasználást megelőzően az új takarmányt, takarmány-alapanyagot, takarmány-kiegészítőanyagot, takarmány-adalékanyagot, valamint a hazai engedéllyel vagy szabvánnyal nem rendelkező import takarmányt a takarmányozási célú hasznosíthatóság szempontjából minősíteni kell. A minősítés iránti kérelmet a minősítő intézethez kell benyújtani, amely a minősítésről határozatot ad ki, ami egyben a termék forgalombahozatali engedélye.
(2) A minősítést megelőző vizsgálatoknak ki kell terjednie
a) a szükséges laboratóriumi vizsgálatokra;
b) szükség szerint az állatetetési kísérletekre.
(3) Gyógyszeres takarmány esetén az engedély a szakértő intézet szakvéleménye alapján adható ki.
(4) A hazai és nemzetközi takarmányozásban ismeretlen, illetve tisztázatlan hatású új takarmányok minősítéséhez a minősítő intézet szakértőt kérhet fel.
Tv.7. § (1) A minősítő intézet kérelem alapján engedélyezheti a nem minősített takarmányok felhasználását
a) kutatómunkák és kísérletek céljára;
b) a takarmányelőállító üzemek által végzett kísérleti programok időtartamára, a takarmány minősítéséig;
c) az állatok létszükségletét biztosító ellátás veszélyeztetése esetén (pl. természeti csapás).
(2) Gyógyszeres takarmány esetében a minősítő intézet a szakértő intézet szakvéleménye alapján adja ki az engedélyt.
(A Tv. 6–7. §-aihoz)
Hazai előállítású új takarmány
A hazai engedéllyel nem rendelkező import takarmányok
A hazai takarmányozási gyakorlatban ismeretlen,
de az Európai Unió tagállamaiban már engedéllyel rendelkező import takarmányok
A takarmány csomagolása és jelölése
Tv.8. § (1) Takarmány-alapanyagot, takarmány-kiegészítőanyagot, takarmány-adalékanyagot, gyógyszeres takarmányt, előkeveréket, takarmánykeveréket, tápot és tápszert csak olyan csomagolóanyagban lehet forgalomba hozni, amely biztosítja a takarmány minőségének megóvását.
(2) A takarmányelőállító üzemben előállított takarmány-alapanyag, illetve takarmány-kiegészítőanyag, takarmány-adalékanyag, gyógyszeres takarmány, előkeverék, takarmánykeverék, táp és tápszer csomagolóanyagán, illetve címkéjén magyarul, jól olvashatóan, eltávolíthatatlanul és észrevehetően fel kell tüntetni a takarmány
a) elnevezését;
b) összetevőinek felsorolását;
c) garantált beltartalmát;
d) a takarmányba kevert gyógyszer nevét, törzskönyvi számát és hatóanyagának a takarmány egységnyi tömegére számított mennyiségét;
e) élelmiszertermelő állat esetében az élelmezés-egészségügyi várakozási időt;
f) rendeltetését;
g) megfelelő alkalmazását lehetővé tevő felhasználási, etetési útmutatót;
h) előállításának időpontját;
i) minőségmegőrzési időtartamát;
j) származását, az előállítás helyét;
k) előállítójának és a forgalmazójának megnevezését;
l) a munkavédelmi előírásokat;
m) a tárolási és raktározási javaslatot;
n) a ,,csak takarmányozási célra'' feliratot.
(3) A takarmányelőállító üzemben előállított ömlesztett takarmány esetében az előállítónak a (2) bekezdésben felsorolt adatokat a takarmány kísérő okmányán kell feltüntetni.
(4) A takarmányelőállító üzemen kívül előállított takarmány-alapanyagok esetében azok csomagolóanyagán, illetve kísérő okmányán fel kell tüntetni:
a) az elnevezést;
b) a rendeltetést;
c) az előállítás időpontját, helyét;
Tv.9. § (1) Belföldi felhasználás vagy forgalomba hozatal céljából kizárólag az e törvény előírásainak megfelelő takarmányt szabad importálni. Az importálni kívánt takarmányt csak a minősítő intézet engedélyével lehet behozni, vámeljárás alá vonni és vámkezeltetni.
(2) Tilos olyan takarmányt importálni, előállítani, forgalomba hozni, forgalmazni és felhasználni, amely Magyarországon nem törzskönyvezett állatgyógyászati készítményt tartalmaz.
A takarmányozási szakigazgatás és a takarmányozási hatóság feladatai
Tv.10. § (1) A takarmány, takarmány-alapanyag, takarmány-kiegészítőanyag, takarmány-adalékanyag, gyógyszeres takarmány, előkeverék, takarmánykeverék, táp és tápszer, szálas- és tömegtakarmány előállításával, importjával, forgalomba hozatalával, forgalmazásával, felhasználásával és vizsgálatával kapcsolatos szabályozási, szervezési, igazgatási és hatósági feladatokat a minisztérium, a takarmányozási hatóság és a takarmányfelügyelő látja el.
(2)
a) A takarmányfelügyelő első fokú határozatát felettes szervként az Állomás vezetője bírálja el.
b) A takarmányozási hatóság vezetőjének első fokú határozatát felettes szervként a minisztérium bírálja el.
(3) A takarmányozási hatóság eljárására az államigazgatási eljárás általános szabályairól szóló 1957. évi IV. törvény rendelkezéseit az e törvényben foglalt eltérésekkel kell alkalmazni.
Tv.11. § (1) A minisztérium
a) irányítja a takarmányminősítési és ellenőrzési tevékenységet;
b) kialakítja a takarmányozásra vonatkozó szabályozást;
c) gondoskodik a takarmányozásra vonatkozó kötelező előírásokat, szakmai irányelveket, ajánlásokat tartalmazó takarmánykódex kialakításáról és közzétételéről;
d) kijelöli és nyilvántartja a hatósági ellenőrzés során vett takarmányminták vizsgálatát végző laboratóriumokat.
(2) A hatósági ellenőrzés során vett takarmányminták vizsgálatára kijelölt laboratóriumokat közzé kell tenni a minisztérium hivatalos lapjában.
(A Tv. 11. §-ához)
A Magyar Takarmánykódex
Tv.12. § A minősítő intézet takarmányozási hatósági jogkörében
a) minősíti:
1. az új takarmányt,
2. a hazai engedéllyel nem rendelkező import takarmányt,
3. a szolgáltatást végző takarmányvizsgáló laboratóriumokat;
b) engedélyezi:
1. a minősített új takarmányok előállítását és forgalomba hozatalát,
2. a nem minősített takarmányok kísérleti jellegű felhasználását,
3. az import termékek takarmányozási célú behozatalát, és forgalomba hozatalát,
4. a szolgáltatást végző takarmányvizsgáló laboratóriumok működését;
c) nyilvántartja, ellenőrzi és irányítja a szolgáltatást végző takarmányvizsgáló laboratóriumokat.
(A Tv. 12. §-ához)
Tv.13. § A szakértő intézet
a) szakvéleményt ad:
1. a takarmányelőállító üzem engedélyezéséhez,
2. az új és import gyógyszeres takarmány forgalomba-hozatali engedélyének kiadásához,
3. a minősítő intézethez benyújtott gyógyszeres takarmányok nyilvántartásba vételéhez,
4. a gyógyszeres takarmányt vizsgáló laboratóriumok engedélyezéséhez;
b) szakmailag irányítja:
1. a gyógyszeres takarmányt vizsgáló laboratóriumok tevékenységét az állatgyógyászati készítmények vonatkozásában,
2. a hatósági ellenőrzés során vett takarmányminták vizsgálatára kijelölt laboratóriumokat;
c) a b) 1., 2. pontban foglaltak végrehajtására körvizsgálatokat szervez;
d) szükség esetén javasolhatja a minősítő intézetnek a gyógyszeres takarmányt vizsgáló laboratóriumok engedélyének visszavonását.
(A Tv. 13. §-ához)
Tv.14. § Az Állomás takarmányozási hatósági jogkörében
a) engedélyezi a természetes állapotú növényi eredetű, illetve szabvánnyal rendelkező alapanyagok kivételével a takarmány-alapanyagot, takarmány-kiegészítőanyagot, nem nutritív testidegen takarmány-kiegészítőanyagot, takarmány-adalékanyagot, gyógyszeres takarmányt, előkeveréket, takarmánykeveréket, tápot és tápszert gyártó takarmányelőállító üzem működését, továbbá az előállítani kívánt takarmányok körét;
b) szakhatósági hozzájárulást ad az a) pontban meghatározott takarmányokat előállító üzem létesítéséhez;
c) nyilvántartja:
1. a takarmányelőállító üzemeket,
2. az előállított takarmányokat és azok gyártmánylapját,
3. a minősített, illetve engedélyezett takarmányokat;
d) ellenőrzi:
1. a takarmányelőállító üzemeket,
2. a takarmány-alapanyagot, takarmány-kiegészítőanyagot, nem nutritív testidegen takarmány-kiegészítőanyagot, takarmány-adalékanyagot, gyógyszeres takarmányt, előkeveréket, takarmánykeveréket, tápot és tápszert és azok előállítását, kezelését, forgalmazását, forgalomba hozatalát, felhasználását és összetételét,
3. a forgalomba hozott és importált szálas- és tömegtakarmányok nem kívánatos, mérgező anyagait;
Tv.15. § (1) Az Állomások takarmányfelügyelői részére szolgálati igazolványt kell adni.
(2) A takarmányfelügyelő jogosult
a) ellenőrizni:
1. a takarmányelőállító üzemeket, importőröket és forgalmazó egységeket,
2. az előállítás személyi és tárgyi feltételeit,
3. a gyártásban felhasznált takarmány-alapanyagot, valamint az előállított takarmányok nyilvántartását, forgalmazását, tárolását;
b) laboratóriumi vizsgálatok céljára térítésmentes mintát venni;
c) a 18. § a), c), d) és f) pontjaiban foglalt hatósági intézkedéseket alkalmazni.
(3) A takarmányfelügyelő beléphet a takarmányelőállító üzem, az importáló, a takarmányforgalmazó területére, továbbá a takarmányt, takarmány-alapanyagot, takarmány-kiegészítőanyagot, takarmány-adalékanyagot, gyógyszeres takarmányt, előkeveréket, takarmánykeveréket, tápot és tápszert árusító üzlethelyiségbe, megtekintheti a dokumentációkat és a ki- és berakodás helyén a szállítóeszközöket.
Tv.16. § Az ellenőrzött természetes személy, illetve az 1. § b) pontjában foglalt gazdálkodó szervezet köteles az ellenőrzéshez szükséges valamennyi adatot, anyagot és eszközt a takarmányozási hatóság rendelkezésére bocsátani.
Hatósági vizsgálatok
Tv.17. § (1) A takarmányozási hatóság által végzett minősítési, engedélyezési és ellenőrzési vizsgálatok díjkötelesek, a díjak mértékét jogszabály állapítja meg. A megállapított díjat a számlát kibocsátó takarmányozási hatóság számára kell befizetni.
(2) A takarmányozási hatóság a minősítés és az ellenőrzés során a helyszínen térítésmentesen mintát vehet. Az ellenőrzött kérésére — a mikrobiológiai vizsgálat céljára vett minta kivételével — ellenmintát kell venni. A mintavételről a helyszínen jegyzőkönyvet kell készíteni.
(A Tv. 15–17. §-aihoz)
Hatósági intézkedések
Tv.18. § (1) Minden olyan esetben, amikor az Állomás az e törvényben, más jogszabályban, előírásban foglaltak megszegését észleli
a) megtilthatja az üzem, berendezés, gép, felszerelés működtetését, illetve a csomagolóanyag felhasználását, továbbá a takarmánytároló hely vagy a szállítóeszköz használatát, kezdeményezheti a takarmányt árusító üzlet működési engedélyének visszavonását;
b) további feltételekhez kötheti az újbóli működtetést, a használatbavételt, illetve használatban tartást;
c) az állat, illetve az ember egészségét veszélyeztető takarmányok forgalomba hozatala, illetve felhasználása esetén a takarmányozási hatóság értesíti az ÁNTSZ területileg illetékes intézetét;
d) a takarmányt etetésre alkalmatlannak nyilvánítja, felhasználását, forgalomba hozatalát korlátozza, feltételhez köti, illetve megtiltja, valamint a környezetvédelmi előírások figyelembevételével elrendeli a megsemmisítését;
e) felfüggeszti, illetve visszavonja a 12—14. §-ban foglalt engedélyeket, kijelölést, minősítést és nyilvántartásba vételt;
f) szabálysértési eljárást kezdeményez.
(2) Az Állomás csökkent értékűnek nyilvánítja azt a takarmányt, amelynek összetevői és beltartalmi értékei a megengedettnél nagyobb mértékben eltérnek a jelölésen, illetve a takarmány kísérő okmányán feltüntetett értékektől, de nem veszélyezteti az állat és az ember egészségét. A takarmányozási hatóság által végrehajtott értékcsökkentés mértékét a felhasználó számára egyértelműen jelezni kell.
(A Tv. 18. §-ához)
Minőségvédelmi bírság
Tv.19. § (1) Ha a vizsgálat során az Állomás megállapítja, hogy az előállított, illetve forgalomba hozott takarmány beltartalmi értékei jogszabályban meghatározott mértéknél nagyobb mértékben eltérnek a garantált beltartalmi értékektől, az előírt szinttől eltérő mértékben gyógyszerhatóanyagot, vagy a maximális szintet meghaladó mértékben nem kívánatos, mérgező anyagot tartalmaz, minőségvédelmi bírságot szab ki.
(2) A minőségvédelmi bírságot a vizsgált tétellel azonos takarmányra lehet kiszabni. A minőségvédelmi bírság összege a vizsgált tétellel azonos takarmány kereskedelmi értékének legalább kétszerese, és legfeljebb tízszerese lehet. A vizsgált tétellel azonos takarmány fogalmát, valamint a minőségvédelmi bírságra vonatkozó előírásokat jogszabály tartalmazza. A minőségvédelmi bírság a 18. § szerinti intézkedések mellett is kiszabható.
(3) A minőségvédelmi bírságot az Állomás folyószámlájára kell befizetni. A befolyt összeg felhasználásáról a takarmányvizsgálati módszerek korszerűsítésére és a takarmányok minőségének javítását elősegítő intézkedésekre figyelemmel a minisztérium dönt.
(A Tv. 19. §-ához)
Felhatalmazások
Tv.20. § (1) Felhatalmazást kap a földművelésügyi miniszter, hogy szabályozza20
a) a takarmány előállításának, importjának, forgalomba hozatalának és felhasználásának, valamint a takarmány minősítésének feltételeit;21
b) a laboratóriumok takarmányvizsgálatára vonatkozó engedélyek kiadásának rendjét;
c) a takarmányba keverhető állatgyógyászati készítmények, takarmány-adalékanyagok használatát, valamint azok nem kívánatos, mérgezőanyag-tartalmának maximális szintjeit a népjóléti miniszter22rel egyetértésben;23
d) a takarmányba, előkeverékbe keverhető biológiailag aktív anyagok használatát, valamint a takarmányok, takarmány-kiegészítőanyagok, beltartalom és gyógyszerhatóanyag-tartalom értékének megengedhető eltéréseit;
e) a tápok és tápszerek minőségi követelményeit;
f) a takarmányozásra vonatkozó szakmai irányelveket, ajánlásokat tartalmazó takarmánykódex kiadásának rendjét;
g) a takarmány-alapanyagot, a takarmány-kiegészítőanyagot és takarmány-adalékanyagot, az előkeveréket, a takarmánykeveréket, a tápot, a tápszert és a gyógyszeres takarmányt előállító üzemek engedélyezését, üzemeltetését, technológiai előírásait;
h) a takarmányminősítés és -ellenőrzés szakmai szabályait, valamint — a pénzügyminiszterrel egyetértésben — a takarmányok hatósági vizsgálatáért fizetendő díjakat;24
i) a minőségvédelmi bírság részletes szabályait.
(2) Felhatalmazást kap a földművelésügyi miniszter, hogy kijelölje a minősítő, illetőleg szakértői feladatokat ellátó intézetet.
Tv.21. § (1) Ez a törvény 1996. július 1. napján lép hatályba, egyidejűleg az ipari takarmányok előállításáról és forgalomba hozataláról szóló 9/1974. (III. 21.) MT, valamint az azt módosító 44/1977. (XI. 19.) MT, az 1/1983. (I. 19.) MT és a 32/1986. (VIII. 21.) MT rendelet hatályát veszti.
(2) A törvény hatálybalépése előtt takarmány-előállításra, forgalomba hozatalra, laboratóriumi tevékenységre kiadott engedélyek továbbra is érvényben maradnak.
1. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
|
Állatfaj, hasznosítási irány, életkor |
ME |
Ny. feh. |
Met. |
M+C |
Lizin |
Ca |
P |
Na |
A |
D3 |
E |
|
|
vitamin |
||||||||||||
|
MJ/kg |
% |
% |
% |
% |
% |
% |
% |
NE/kg |
mg/kg |
|||
|
Broiler indítótáp (0—3 hét) |
12,5 |
21,0 |
0,50 |
0,85 |
1,1 |
0,9 |
0,6 |
0,12 |
6 000 |
1 000 |
10 |
|
|
Broiler nevelőtáp (3—6 hét) |
12,6 |
19,0 |
0,40 |
0,75 |
1,0 |
0,7 |
0,6 |
0,12 |
6 000 |
1 000 |
10 |
|
|
Broiler befejezőtáp (6—7 hét) |
12,6 |
17,0 |
0,30 |
0,60 |
0,8 |
0,7 |
0,5 |
0,12 |
5 000 |
750 |
7,5 |
|
|
Jérce indítótáp (0—6 hét) |
11,5 |
18,0 |
0,35 |
0,65 |
0,9 |
1,0 |
0,6 |
0,11 |
6 000 |
1 000 |
10 |
|
|
Jérce nevelőtáp 1. (6—12 hét) |
11,0 |
15,0 |
0,30 |
0,50 |
0,6 |
1,0 |
0,5 |
0,11 |
4 000 |
750 |
10 |
|
|
Jérce nevelőtáp 2. (12—18 hét) |
10,5 |
13,0 |
0,25 |
0,40 |
0,5 |
1,0 |
0,5 |
0,11 |
3 500 |
700 |
10 |
|
|
Tojó előkészítőtáp (18—első tojásig) |
11,0 |
16,0 |
0,30 |
0,50 |
0,6 |
2,0 |
0,6 |
0,11 |
6 000 |
1 000 |
10 |
|
|
Tojótáp I. (70% termelés felett) |
11,0 |
16,0 |
0,30 |
0,50 |
0,7 |
3,5 |
0,6 |
0,13 |
6 000 |
1 000 |
10 |
|
|
Tojótáp II. (70% termelés alatt) |
11,0 |
15,0 |
0,25 |
0,45 |
0,6 |
3,5 |
0,6 |
0,13 |
6 000 |
1 000 |
10 |
|
|
Tenyésztojótáp |
11,5 |
16,0 |
0,30 |
0,50 |
0,7 |
3,2 |
0,5 |
0,13 |
10 000 |
1 500 |
15 |
|
|
Pulyka indítótáp (0—4 hét) |
11,7 |
26,0 |
0,55 |
1,00 |
1,5 |
1,2 |
0,8 |
0,14 |
10 000 |
2 000 |
15 |
|
|
Pulyka nevelőtáp I. (4—8 hét) |
12,1 |
23,0 |
0,45 |
0,85 |
1,3 |
1,0 |
0,7 |
0,14 |
8 000 |
1 500 |
12 |
|
|
Pulyka nevelőtáp II. (8—12 hét) |
12,3 |
21,0 |
0,40 |
0,72 |
1,1 |
1,0 |
0,6 |
0,14 |
8 000 |
1 500 |
10 |
|
|
Pulyka befejezőtáp I. (12—16 hét) |
12,4 |
18,0 |
0,35 |
0,63 |
0,8 |
0,9 |
0,6 |
0,12 |
5 000 |
1 000 |
10 |
|
|
Pulyka befejezőtáp II. (16—vágásig) |
12,5 |
16,0 |
0,30 |
0,54 |
0,7 |
0,9 |
0,6 |
0,12 |
5 000 |
1 000 |
10 |
|
|
Állatfaj, hasznosítási irány, életkor |
ME |
Ny. feh. |
Ny. rost |
Met. |
M+C |
Lizin |
Ca |
P |
Na |
A |
D3 |
E |
|
|
vitamin |
|||||||||||||
|
MJ/kg |
% |
% |
% |
% |
% |
% |
% |
% |
NE/kg |
mg/kg |
|||
|
Pecsenyeliba indítótáp (0—3 hét) |
11,5 |
20,0 |
3,0 |
0,45 |
0,80 |
1,00 |
1,00 |
0,60 |
0,13 |
6 000 |
1 000 |
10 |
|
|
Pecsenyeliba nevelőtáp (3—5 hét) |
11,7 |
17,0 |
4,0 |
0,35 |
0,60 |
0,85 |
0,90 |
0,60 |
0,13 |
6 000 |
1 000 |
10 |
|
|
Pecsenyeliba befejezőtáp (5—8 hét) |
12,0 |
15,0 |
4,5 |
0,30 |
0,50 |
0,60 |
0,80 |
0,60 |
0,13 |
5 000 |
750 |
7,5 |
|
|
Lúd tojótáp |
11,0 |
15,0 |
4,5 |
0,26 |
0,50 |
0,65 |
2,50 |
0,60 |
0,14 |
8 000 |
1 500 |
15 |
|
|
Kacsa indítótáp (0—2 hét) |
12,0 |
18,0 |
3,0 |
0,40 |
0,75 |
1,00 |
0,90 |
0,60 |
0,14 |
6 000 |
1 000 |
10 |
|
|
Kacsa hizlalótáp (2—7 hét) |
12,2 |
15,5 |
3,5 |
0,30 |
0,60 |
0,70 |
0,90 |
0,60 |
0,14 |
6 000 |
1 000 |
10 |
|
|
Kacsa tojótáp |
11,2 |
15,0 |
4,0 |
0,35 |
0,60 |
0,70 |
2,70 |
0,60 |
0,14 |
10 000 |
2 000 |
15 |
|
|
Állatfaj, hasznosítási irány, életkor |
DEs |
Ny. feh. |
Lizin |
M+C |
Ca |
P |
Na |
A |
D3 |
E |
|
vitamin |
||||||||||
|
MJ/kg |
% |
% |
% |
% |
% |
% |
NE/kg |
mg/kg |
||
|
Vemheskocatáp |
12,0 |
12,3 |
0,54 |
0,35 |
0,94 |
0,67 |
0,12 |
7500 |
1000 |
20 |
|
Szoptatókocatáp |
13,0 |
15,9 |
0,78 |
0,51 |
1,09 |
0,78 |
0,12 |
8000 |
1000 |
20 |
|
Tenyészkantáp |
12,4 |
15,0 |
0,61 |
0,40 |
0,74 |
0,50 |
0,16 |
8000 |
1000 |
20 |
|
Szopósmalac-táp |
14,0 |
20,0 |
1,24 |
0,74 |
0,90 |
0,70 |
0,10 |
8000 |
1200 |
25 |
|
Malactáp I. |
13,8 |
18,3 |
1,10 |
0,66 |
0,80 |
0,60 |
0,10 |
7000 |
1100 |
20 |
|
Malactáp II. |
13,7 |
17,3 |
0,95 |
0,57 |
0,80 |
0,60 |
0,10 |
6500 |
900 |
15 |
|
Hízósertéstáp I. |
13,0 |
15,5 |
0,80 |
0,48 |
0,70 |
0,55 |
0,12 |
3500 |
500 |
10 |
|
Hízósertéstáp II. |
13,0 |
14,5 |
0,70 |
0,42 |
0,60 |
0,50 |
0,12 |
3000 |
400 |
10 |
|
Hízósertéstáp III. |
13,0 |
13,5 |
0,65 |
0,39 |
0,60 |
0,45 |
0,12 |
2500 |
250 |
10 |
|
Tenyészsüldőtáp I. |
12,5 |
16,3 |
0,85 |
0,51 |
0,85 |
0,63 |
0,12 |
4500 |
600 |
15 |
|
Tenyészsüldőtáp II. |
12,5 |
14,9 |
0,75 |
0,49 |
0,75 |
0,54 |
0,12 |
4000 |
500 |
15 |
2. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
cégszerű aláírása
3. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
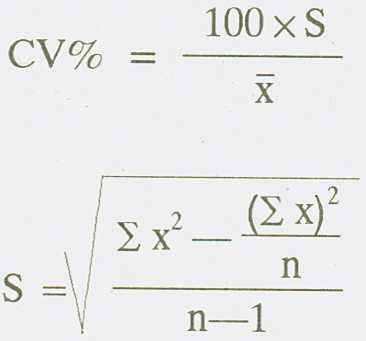
4. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
és a vizsgálatok elvárt variációs koefficiens értéke az előírt hatóanyagcsoportok vonatkozásában
|
Takarmánycsoportok megnevezése |
A mintában vizsgálandó paraméterek |
CV% maximum |
|
Vitamin, mikroelem és egységes premix |
Vitaminok, illetve mikroelemek vonatkozásában min. 2 paraméter, amennyiben állatgyógyászati készítményt is tartalmaz max. 4 hatóanyag |
5% |
|
Komplett premix |
Nyomelemek, makroelemek vonatkozásában min. 2 paraméter, amennyiben állatgyógyászati készítményt is tartalmaz max. 4 hatóanyag |
8% |
|
Koncentrátum |
Nyomelemek, makroelemek vonatkozásában min. 2 paraméter, amennyiben állatgyógyászati készítményt is tartalmaz max. 4 hatóanyag |
10% |
|
Táp, takarmánykeverék és tápszer |
Nyomelemek, makroelemek vonatkozásában min. 2 paraméter, amennyiben állatgyógyászati készítményt is tartalmaz max. 4 hatóanyag |
12% |
5. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
6. számú melléklet a 25/1996. (IX. 4.) FM rendelethez25
7. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
|
Mikroelemek |
Állatfaj vagy korcsoport |
A mindenkori szárazanyag-tartalomra vonat- |
|
Vas |
minden állatfaj |
1250 |
|
Jód |
lófélék |
4 összesen |
|
|
egyéb állatfajok és korcsoportjai |
40 összesen |
|
Kobalt |
minden állatfaj |
10 összesen |
|
Réz |
borjak |
30 tejpótló tápszerekben |
|
|
juhok |
15 |
|
|
hízósertések 16 hétig |
175 |
|
|
hízósertések 16 hét felett |
35 |
|
|
tenyészsertések |
35 |
|
|
egyéb állatfajok és korcsoportjaik |
35 összesen |
|
Mangán |
minden állatfaj |
250 összesen |
|
Molibdén |
minden állatfaj |
2,5 összesen |
|
Szelén |
minden állatfaj |
0,5 összesen |
|
Cink |
minden állatfaj |
250 összesen |
8. számú melléklet a 25/1996. (IX. 4.) FM rendelethez26
9. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
10. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
|
Megnevezés |
Mértékegység |
Táp, koncentrátum, |
Előkeverékek a |
Tápszer |
|
Nedvesség maximum |
% |
+ |
+ |
+ |
|
Nyersfehérje minimum |
% |
+ |
+ |
+ |
|
ebből NPN/maximum |
% |
+ |
+ |
|
|
Nyerszsír minimum |
% |
+ |
|
+ |
|
Nyersrost maximum |
% |
+ |
|
|
|
Metionin minimum |
% |
+ |
+ |
+ |
|
Lisin minimum |
% |
+ |
+ |
+ |
|
Met. + Cisztin minimum |
% |
+ |
+ |
+ |
|
Nátrium minimum |
% |
+ |
+ |
+ |
|
Kálcium minimum |
% |
+ |
+ |
+ |
|
Foszfor minimum |
% |
+ |
+ |
+ |
|
Cink minimum |
mg/kg |
|
+ |
+ |
|
Réz minimum |
mg/kg |
|
+ |
+ |
|
Vas minimum |
mg/kg |
|
+ |
+ |
|
Mangán minimum |
mg/kg |
|
+ |
+ |
|
Jód minimum |
mg/kg |
|
|
+ |
|
Kobalt minimum |
mg/kg |
|
|
+ |
|
Szelén |
mg/kg |
|
+ |
+ |
|
A-vitamin |
NE/kg |
+ |
+ |
+ |
|
D-vitamin |
NE/kg |
+ |
+ |
+ |
|
E-vitamin |
mg/kg |
+ |
+ |
+ |
|
Számított energiaértékek (állatfajnak megfelelően) minimum |
MJ/kh |
+ |
|
+ |
|
K-vitamin minimum |
mg/kg |
|
+ |
|
|
B1-vitamin minimum |
mg/kg |
|
+ |
|
|
B2-vitamin minimum |
mg/kg |
|
+ |
|
|
Pantoténsav minimum |
mg/kg |
|
+ |
|
|
Kolinklorid minimum |
mg/kg |
|
+ |
|
|
Nikotinsav minimum |
mg/kg |
|
+ |
|
|
B6-vitamin minimum |
mg/kg |
|
+ |
|
|
B12-vitamin minimum |
mg/kg |
|
+ |
|
|
Biotin minimum |
mg/kg |
|
+ |
|
|
C-vitamin minimum |
mg/kg |
|
+ |
|
|
Savfok maximum |
SH° |
|
|
+ |
|
Oldhatósági max. index |
|
|
|
+ |
11. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
megengedhető eltérések
|
Vizsgált paraméterek |
Értékhatárok |
Megengedhető eltérések |
|
Nedvességtartalom |
5%-ig |
0,5% A |
|
5–10% között |
10,0% R |
|
|
10–20% között |
1,0% A |
|
|
20% felett |
5,0% R |
|
|
Nyersfehérje-tartalom |
10%-ig |
1,0% A |
|
10–20% között |
10,0% R |
|
|
20% felett |
2,0% A |
|
|
Emészthető nyersfehérje-tartalom |
10%-ig |
2,0% A |
|
10–20% között |
20,0% R |
|
|
20% felett |
4,0% A |
|
|
Energiatartalom |
10 MJ/kg |
10,0% R |
|
10 MJ/kg |
1,0% A |
|
|
Nyerszsírtartalom |
8%-ig |
0,8% A |
|
8–15% között |
10,0% R |
|
|
15% felett |
1,5% A |
|
|
Nyersrosttartalom |
6%-ig |
1,5% A |
|
6–12% között |
25,0% R |
|
|
12% felett |
3,0% A |
|
|
Keményítőtartalom |
|
3,0% A |
|
Nyershamutartalom |
5%-ig |
0,8% A |
|
5–10% között |
16,0% R |
|
|
10% felett |
1,6% A |
|
|
Sósavban oldhatatlan hamu-(homok-)tartalom |
4%-ig |
0,6% A |
|
4–10% között |
15,0% R |
|
|
10% felett |
1,5% A |
|
|
Kálium-, magnézium-, nátriumtartalom |
0,2%-ig |
0,06% A |
|
0,2–1,0% között |
30,0% R |
|
|
1,0–2,0% között |
0,3% A |
|
|
2,0% felett |
15,0% R |
|
|
Calcium-, foszfortartalom |
1%-ig |
0,3% A |
|
1–2% között |
30,0% R |
|
|
2–5% között |
0,6% A |
|
|
5% felett |
12,0% R |
|
|
Réz-, kobalt-, vas-, mangán-, cinktartalom |
30 mg/kg-ig |
15,0 mg/kg A |
|
30 mg/kg– 50 mg/kg között |
50,0% R |
|
|
50 mg/kg–100 mg/kg között |
25,0 mg/kg A |
|
|
100 mg/kg felett |
25,0% R |
|
|
Szeléntartalom |
0,5 mg/kg-ig |
70,0% R |
|
0,5 mg/kg– 1,0 mg/kg között |
0,35 mg/kg A |
|
|
1,0 mg/kg–10,0 mg/kg között |
35,0% R |
|
|
10,0 mg/kg–14,0 mg/kg között |
3,50 mg/kg A |
|
|
14,0 mg/kg felett |
25,0% R |
|
|
Jódtartalom |
|
40,0% R |
|
Lizin-, Metionin-, Treonintartalom |
|
15,0% R |
|
Cisztin-, Triptofántartalom |
|
20,0% R |
|
A-vitamin-tartalom |
10 000 NE/kg-ig |
40,0% R |
|
10 000 NE/kg– 20 000 NE/kg között |
4000 NE/kg A |
|
|
20 000 NE/kg–100 000 NE/kg között |
20,0% R |
|
|
100 000 NE/kg–125 000 NE/kg között |
20 000 NE/kg A |
|
|
125 000 NE/kg között |
16,0% R |
|
|
D-vitamincsoport-tartalom |
3 000 NE/kg-ig |
60,0% R |
|
3 000 NE/kg– 6 000 NE/kg között |
1 800 NE/kg A |
|
|
6 000 NE/kg– 60 000 NE/kg között |
30,0% R |
|
|
60 000 NE/kg–100 000 NE/kg között |
18 000 NE/kg A |
|
|
100 000 NE/kg felett |
18,0% R |
|
|
E-vitamin-tartalom |
150 mg/kg-ig |
30,0% R |
|
150 mg/kg–180 mg/kg között |
450 mg/kg A |
|
|
180 mg/kg–400 mg/kg között |
25,0% R |
|
|
400 mg/kg–800 mg/kg között |
100,0 mg/kg A |
|
|
800 mg/kg felett |
12,5% R |
|
|
K-vitamin-(Menadion-)tartalom |
100 mg/kg-ig |
40,0% R |
|
100 mg/kg–200 mg/kg között |
40,0 mg/kg A |
|
|
200 mg/kg felett |
20,0% |
|
|
Egyéb vitamintartalom |
150 mg/kg-ig |
40,0% R |
|
150 mg/kg–250 mg/kg között |
60,0 mg/kg A |
|
|
250 mg/kg felett |
24,0% R |
|
|
Gyógyszerhatóanyag-tartalom |
5 mg/kg-ig |
40,0% R |
|
5 mg/kg– 10 mg/kg között |
2,0 mg/kg A |
|
|
10 mg/kg–100 mg/kg között |
20,0% R |
|
|
100 mg/kg–125 mg/kg között |
20,0 mg/kg A |
|
|
125 mg/kg–500 mg/kg között |
16,0% R |
|
|
500 mg/kg–800 mg/kg között |
80,0 mg/kg A |
|
|
800 mg/kg felett |
10,0% R |
|
Vizsgált paraméterek |
Értékhatárok |
Megengedhető eltérések |
|
Nedvességtartalom |
20,0%-ig |
1,5% A |
|
20,0–40,0% között |
7,5% R |
|
|
40,0% felett |
3,0% A |
|
|
Nyersfehérje-tartalom |
12,5%-ig |
2,0% A |
|
12,5%–20,0% között |
16,0% R |
|
|
20,0% felett |
3,2% A |
|
|
Nyerszsírtartalom |
|
2,5% A |
|
Nyersrosttartalom |
|
3,0% A |
|
Nyershamutartalom |
|
4,5% A |
12. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
INTÉZET
neve és postacíme
13. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
14. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
INTÉZET
neve és postacíme
15. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
INTÉZET
neve és postacíme
16. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
INTÉZET
neve és postacíme
17. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
de az Európai Unió tagállamaiban már engedéllyel rendelkező import takarmányok behozatalának, forgalomba hozatalának, forgalmazásának és takarmányozási célú felhasználásának engedélyezése iránti kérelem
INTÉZET
cégszerű aláírása neve és postacíme
18. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
de az Európai Unió tagállamaiban engedélyezett, illetve engedélyezés alatt álló hasznos mikroorganizmusokat tartalmazó készítmények behozatalának, forgalomba hozatalának, forgalmazásának és takarmányozási célú felhasználásának engedélyezése iránti kérelem
INTÉZET
neve és postacíme
19. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
de az Európai Unió tagállamaiban engedélyezett, illetve engedélyezés alatt álló enzimkészítmények behozatalának, forgalomba hozatalának, forgalmazásának és takarmányozási célú felhasználásának engedélyezése iránti kérelem
INTÉZET
neve és postacíme
20. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
21. számú melléklet a 25/1996. (IX. 4.) FM rendelethez
|
Vizsgált paraméterek |
Méréstartomány |
Eltérés |
|
Nedvesség |
<= 15% |
+- 0,3% A |
|
> 15% |
+- 2,0% R |
|
|
Nyersfehérje |
<= 16% |
+- 0,4% A |
|
> 16 <= 32% |
+- 2,5% R |
|
|
> 32% |
+- 0,8% A |
|
|
Emészthető nyersfehérje |
<= 16% |
+- 0,8% A |
|
> 16 <= 50% |
+- 5% R |
|
|
> 50% |
+- 2,5% A |
|
|
Nyerszsír |
<= 10% |
+- 0,4% A |
|
> 10 <= 20% |
+- 4,0% R |
|
|
> 20% |
+- 0,8% A |
|
|
Nyersrost |
<= 10% |
+- 0,4% A |
|
> 10% |
+- 4,0% R |
|
|
Nyershamu |
<= 10% |
+- 0,4% A |
|
> 10 <= 15% |
+- 4,0% R |
|
|
> 15 <= 20% |
+- 0,6% A |
|
|
> 20% |
+- 3,0% R |
|
|
Sósavban oldhatatlan hamu |
<= 10% |
+- 0,3% A |
|
Oldhatósági index |
|
+- 10% R |
|
Só |
<= 1,5% |
+- 0,2% A |
|
> 1,5 <= 5% |
+- 0,4% A |
|
|
> 5,0% |
+- 0,5% A |
|
|
Ca |
<= 0,5% |
+- 0,05% A |
|
P |
> 0,5 <= 6% |
+- 10% R |
|
> 6 <= 10% |
+- 0,6% A |
|
|
> 10% |
+- 6% R |
|
|
K |
<= 16/ |
+- 0,02% A |
|
Mg |
> 0,16 <= 8% |
+- 12,5% R |
|
Na |
> 8% |
+- 1,0% A |
|
Összes foszfor, citromsavban, semleges és alkálikus ammónium-citrátban oldható foszfor |
<= 5% |
az átlag 3%-a R |
|
> 5% |
+- 0,20% A |
|
|
Karbonáttartalom |
<= 5% |
+- 0,1% A |
|
> 5 <= 25% |
+- 0,2% A |
|
|
> 25% |
+- 0,5% A |
|
|
Mikroelemek |
<= 30 mg/kg |
+- 9 mg/kg A |
|
Se |
<= 0,5 mg/kg |
+- 40% R |
|
> 0,5 <= 1 mg/kg |
+- 0,2 mg/kg A |
|
|
> 1 <= 10 mg/kg |
+- 20% A |
|
|
> 10 <= 20 mg/kg |
+- 2 mg/kg A |
|
|
> 20 mg/kg |
+- 10% R |
|
|
Jód |
|
+- 25% R |
|
Összes cukortartalom |
<= 25% |
+- 2% A |
|
Keményítőtartalom |
<= 12% |
+- 0,6% A |
|
> 12 <= 20% |
+- 5% R |
|
|
> 20% |
+- 1% A |
|
|
Karbamidtartalom |
<= 2% |
+- 0,3% A |
|
> 2% |
+- 10% R |
|
|
Aminósav-tartalom |
|
+- 15% R |
|
Nitrát-nitrit tartalom |
|
+- 10% R |
|
Karotin |
|
+- 20% R |
|
Xantophyll-tartalom |
|
+- 20% R |
|
Olajos magvak és darák ITC- és VTO-tartalma |
|
+- 20% R |
|
Szója és szójakészítmények tripszininhibitor aktivitása |
|
+- 10% R |
|
A-vitamin |
<= 10 000 NE/kg |
+- 25% R |
|
> 10 000 <= 20 000 NE/kg |
+- 2500 NE/kg A |
|
|
> 20 000 <= 100 000 NE/kg |
+- 12,5% R |
|
|
> 100 000 <= 125 000 NE/kg |
+- 12 500 NE/kg A |
|
|
> 125 000 NE/kg |
+- 10% R |
|
|
D-vitamin |
<= 3 000 NE/kg |
+- 50% R |
|
> 3 000 <= 6 000 NE/kg |
+- 1 500 NE/kg A |
|
|
> 6 000 <= 40 000 NE/kg |
+- 25,0% R |
|
|
> 40 000 <= 100 000 NE/kg |
+- 10 000 NE/kg A |
|
|
> 100 000 NE/kg |
+- 10% R |
|
|
E-vitamin |
<= 150 mg/kg |
+- 20% R |
|
> 150 <= 200 mg/kg |
+- 30 mg/kg A |
|
|
> 200 <= 500 mg/kg |
+- 15% R |
|
|
> 500 <= 750 mg/kg |
+- 75 mg/kg A |
|
|
> 750 mg/kg |
+- 10% R |
|
|
K3-vitamin (Menadion) |
<= 100 mg/kg |
+- 25% R |
|
> 100 <= 250 mg/kg |
+- 25 mg/kg A |
|
|
> 250 mg/kg |
+- 10% R |
|
|
Egyéb vitaminok |
<= 150 mg/kg |
+- 20% R |
|
> 150 <= 200 mg/kg |
+- 30 mg/kg A |
|
|
> 200 mg/kg |
+- 15% R |
|
|
Antioxidáns-tartalom |
|
+- 25% R |
|
Gyógyszertartalom |
<= 5 mg/kg |
+- 30% R |
|
> 5 <= 10 mg/kg |
+- 1,5 mg/kg A |
|
|
> 10 <= 100 mg/kg |
+- 15% R |
|
|
> 100 <= 125 mg/kg |
+- 15 mg/kg A |
|
|
> 125 <= 500 mg/kg |
+- 12% R |
|
|
> 500 <= 750 mg/kg |
+- 60 mg/kg A |
|
|
> 750 mg/kg |
+- 8% R |
|
|
Növényvédőszer-maradék |
<= 1 mg/kg |
+- 50% R |
|
> 1 <= 2,5 mg/kg |
+- 0,5 mg/kg A |
|
|
> 2,5 mg/kg |
+- 20% R |
|
|
Aflatoxin B1 |
<= 4mg/kg |
+- 50% R |
|
> 4 <= 10 mg/kg |
+- 2 mg/kg A |
|
|
> 10 mg/kg |
+- 20% R |
|
|
Mikotoxinok |
<= 0,1 mg/kg |
+- 60% R |
|
> 0,1 <= 0,3 mg/kg |
+- 0,06 mg/kg A |
|
|
> 0,3 <= 1,0 mg/kg |
+- 20% R |
|
|
> 1,0 <= 2,0 mg/kg |
+- 0,2 mg/kg A |
|
|
> 2,0 mg/kg |
= 10% R |
|
|
Toxikus elemek |
|
|
|
As |
<= 1 mg/kg |
+- 50% R |
|
> 1 <= 2,5 mg/kg |
+- 0,5 mg/kg A |
|
|
> 2,5 <= 15 mg/kg |
+- 20% R |
|
|
> 15 <= 30 mg/kg |
+- 3,0 mg/kg A |
|
|
> 30 mg/kg |
+- 10% R |
|
|
Hg |
<= 0,06 mg/kg |
+- 50% R |
|
> 0,06 <= 0,1 mg/kg |
+- 0,03 mg/kg A |
|
|
> 0,1 <= 0,2 mg/kg |
+- 30% R |
|
|
> 0,2 <= 0,3 mg/kg |
+- 0,06 mg/kg A |
|
|
> 0,3 mg/kg |
+- 20% R |
|
|
Cd |
<= 0,2 mg/kg |
+- 50% R |
|
> 0,2 <= 0,4 mg/kg |
+- 0,1 mg/kg A |
|
|
> 0,4 <= 1,0 mg/kg |
+- 25% R |
|
|
> 1,0 <= 2,5 mg/kg |
+- 0,25 mg/kg A |
|
|
> 2,5 mg/kg |
+- 10% R |
|
|
Pb |
<= 3 mg/kg |
+- 50% R |
|
> 3 <= 5 mg/kg |
+- 1,5 mg/kg A |
|
|
> 5 <= 10 mg/kg |
+- 30% R |
|
|
> 10 <= 20 mg/kg |
+- 3 mg/kg A |
|
|
> 20 <= 40 mg/kg |
+- 15% R |
|
|
> 40 <= 60 mg/kg |
+- 6 mg/kg A |
|
|
> 60 mg/kg |
+- 10% R |
|
|
F |
<= 60 mg/kg |
+- 12 mg/kg A |
|
> 60 <= 500 mg/kg |
+- 20% R |
|
|
> 500 <= 1000 mg/kg |
+- 100 mg/kg A |
|
|
> 1000 mg/kg |
+- 10% R |
|
|
Glükozinolát-tartalom (Palládium-kloridos módszer) |
|
+- 5 mm/g A |
|
Csillagfürt alkaloidatartalom |
|
+- 20% R |
|
Ureáz aktivitástartalom |
|
+- 20% R |
|
Peroxidszám, savszám |
|
+- 15% R |
|
Savfok |
|
|
|
– tejpor |
|
+- 5° SH A |
|
– visszaállított tej |
|
+- 0,2° SH A |
|
Szabad zsírsavak |
|
+- 10% R |
22. számú melléklet a 25/1996. (IX. 4.) FM rendelethez38
|
|
Nedvesség |
Energia |
Nyers |
Nyers rost |
Amino- |
Ca |
P |
Na |
Eszenciális nyomelemek nyomelemenként |
|||
|
Többlet |
Hiány |
Hiány |
Hiány |
Többlet |
Hiány |
Hiány |
Hiány |
Hiány |
Többlet |
Hiány |
Toxikus szint |
|
|
Tenyészsüldő, koca, kan |
5 |
6 |
13 |
|
|
10 |
10 |
10 |
5 |
– |
8 |
60 |
|
Malac 30 kg-ig |
5 |
6 |
15 |
|
|
12 |
8 |
8 |
6 |
8 |
9 |
60 |
|
Hízósertés 30–60 kg-ig |
5 |
6 |
10 |
|
|
9 |
6 |
6 |
5 |
– |
8 |
60 |
|
Hízósertés 60 kg felett |
5 |
6 |
8 |
|
|
7 |
6 |
6 |
5 |
– |
7 |
60 |
|
Egyéb sertés |
6 |
6 |
6 |
|
|
7 |
6 |
6 |
5 |
– |
7 |
60 |
|
Baromfi (szárnyas), indító, nevelő (hizlaló) |
6 |
13 |
15 |
|
|
12 |
8 |
8 |
6 |
6 |
7 |
60 |
|
Baromfi (szárnyas) befejező |
6 |
10 |
10 |
|
|
9 |
6 |
6 |
5 |
6 |
5 |
60 |
|
Baromfi (szárnyas), jérce, tojó előkészítő |
6 |
6 |
8 |
|
|
8 |
10 |
9 |
5 |
6 |
6 |
60 |
|
Baromfi (szárnyas) tojó |
6 |
6 |
8 |
|
|
8 |
13 |
9 |
5 |
7 |
6 |
60 |
|
Egyéb baromfi (szárnyas) |
6 |
8 |
10 |
|
|
8 |
8 |
8 |
5 |
6 |
6 |
60 |
|
Borjú, bárány indító |
4 |
6 |
10 |
5 |
0 |
7 |
6 |
6 |
5 |
– |
5 |
60 |
|
Kérődző növendék, hízó |
4 |
5 |
6 |
0 |
0 |
0 |
6 |
6 |
5 |
– |
5 |
60 |
|
Tehén, egyéb kérődző |
4 |
5 |
6 |
0 |
0 |
0 |
8 |
8 |
5 |
– |
6 |
60 |
|
Egyéb kérődző |
4 |
5 |
6 |
0 |
0 |
0 |
6 |
6 |
5 |
– |
5 |
60 |
|
Nyúl, egyéb prémes állat |
4 |
5 |
7 |
10 |
0 |
6 |
6 |
6 |
5 |
– |
5 |
60 |
|
Ló |
5 |
5 |
7 |
5 |
0 |
0 |
6 |
6 |
5 |
– |
5 |
60 |
|
Hal |
0 |
0 |
10 |
0 |
0 |
8 |
6 |
6 |
5 |
– |
5 |
60 |
|
Hobbi állatok |
4 |
0 |
8 |
5 |
5 |
7 |
8 |
8 |
5 |
– |
5 |
60 |
|
Egyéb állatok |
5 |
5 |
8 |
5 |
5 |
7 |
6 |
6 |
5 |
– |
5 |
60 |
|
|
Karbamid |
Vitaminok vitami- |
Gyógyszer- hatóanyagonként |
Mikro- |
Avasság |
Salmonella |
Nem kívánatos, mérgező, valamint tiltott anyagok anyagonként |
Összetételben nem szereplő, nem mérgező idegen anyagok anyagonként, 10%-onként |
||
|---|---|---|---|---|---|---|---|---|---|---|
|
Hiány |
Többlet |
Hiány |
Hiány |
Többlet |
Kifogásolt |
Kifogásolt |
Kifogásolt |
Toxikus |
Kifogásolt |
|
|
Tenyészsüldő, koca, kan |
0 |
25 |
10 |
13 |
15 |
15 |
10 |
60 |
60 |
10 |
|
Malac 30 kg-ig |
0 |
30 |
15 |
15 |
15 |
15 |
10 |
60 |
60 |
15 |
|
Hízósertés 30–60 kg-ig |
0 |
25 |
10 |
10 |
10 |
10 |
8 |
60 |
60 |
10 |
|
Hízósertés 60 kg felett |
0 |
25 |
7 |
10 |
10 |
10 |
8 |
60 |
60 |
10 |
|
Egyéb sertés |
0 |
25 |
7 |
10 |
10 |
10 |
8 |
60 |
60 |
10 |
|
Baromfi (szárnyas), indító, |
0 |
30 |
15 |
15 |
20 |
20 |
15 |
60 |
60 |
15 |
|
Baromfi (szárnyas) befejező |
0 |
30 |
10 |
10 |
10 |
15 |
15 |
60 |
60 |
15 |
|
Baromfi (szárnyas), jérce, |
0 |
30 |
10 |
10 |
15 |
15 |
10 |
60 |
60 |
15 |
|
Baromfi (szárnyas) tojó |
0 |
30 |
8 |
10 |
15 |
15 |
10 |
60 |
60 |
15 |
|
Egyéb baromfi (szárnyas) |
0 |
30 |
8 |
10 |
15 |
15 |
10 |
60 |
60 |
15 |
|
Borjú, bárány indító |
6 |
10 |
8 |
10 |
10 |
10 |
8 |
60 |
60 |
10 |
|
Kérődző növendék, hízó |
7 |
6 |
5 |
8 |
8 |
8 |
7 |
60 |
60 |
5 |
|
Tehén, egyéb kérődző |
7 |
6 |
5 |
8 |
8 |
8 |
7 |
60 |
60 |
8 |
|
Egyéb kérődző |
6 |
6 |
5 |
8 |
8 |
8 |
7 |
60 |
60 |
5 |
|
Nyúl, egyéb prémes állat |
0 |
25 |
6 |
10 |
10 |
10 |
8 |
60 |
60 |
8 |
|
Ló |
0 |
20 |
6 |
15 |
15 |
15 |
10 |
60 |
60 |
10 |
|
Hal |
0 |
20 |
8 |
15 |
15 |
5 |
8 |
60 |
60 |
5 |
|
Hobbi állatok |
0 |
30 |
10 |
15 |
15 |
10 |
15 |
60 |
60 |
10 |
|
Egyéb állatok |
0 |
30 |
8 |
10 |
10 |
10 |
8 |
60 |
60 |
8 |
|
Vizsgálati paraméterek |
|
Hibaértékek |
|---|---|---|
|
Szárazanyag |
hiány |
7 |
|
Nyersfehérje |
hiány |
15 |
|
Emészthető nyersfehérje |
hiány |
15 |
|
Nyerszsír |
hiány |
7 |
|
Nyersrost |
hiány |
5 |
|
Nyershamu |
többlet |
6 |
|
Sósavban oldhatatlan hamu, homok |
többlet |
7 |
|
Oldhatósági index |
kifogásolt |
5 |
|
Na, K |
hiány |
6 |
|
Ca, Mg |
hiány |
9 |
|
P |
hiány |
9 |
|
Savfok |
kifogásolt |
10 |
|
Esszenciális nyomelemek elemenként |
hiány |
10 |
|
Karbamid |
hiány |
5 |
|
Lizin, Metionin, Cisztin, aminosavanként |
hiány |
15 |
|
Egyéb aminósavak, aminosavanként |
hiány |
10 |
|
Vitaminok, vitaminonként |
hiány |
15 |
|
Gyógyszer-hatóanyagok, hatóanyagonként |
hiány |
15 |
|
Avasság |
kifogásolt |
25 |
|
Mikrobiológiai állapot |
kifogásolt |
25 |
|
Szalmonella |
kifogásolt |
60 |
|
Ureáz aktivitás |
kifogásolt |
25 |
|
Káros, mérgező, toxikus anyagok határérték feletti jelenléte, toxikus anyagonként |
toxikus |
60 |
|
Nem káros, nem mérgező, nem toxikus idegen anyag jelenléte, anyagonként, 10%-onként |
|
15 |
|
Jellemző összetevők hiánya 10%-onként |
|
15 |
A törvényt az Országgyűlés az 1995. október 24-i ülésnapján fogadta el. Kihirdetés napja: 1995. november 4. A törvényt a 2001: CXIX. törvény 17. § (3) bekezdése hatályon kívül helyezte 2002. június 1. napjával.
A Vhr. 8. § (2) bekezdése a 45/2001. (VI. 25.) FVM rendelet 1. §-ával megállapított szöveg.
A Vhr. 9. § (1) bekezdése a 45/2001. (VI. 25.) FVM rendelet 2. §-ával megállapított szöveg.
A 9. § (1) bekezdésének b) pontját a 45/2001. (VI. 25.) FVM rendelet 12. § (1) bekezdése alapján 2001. szeptember 1-jétől kell alkalmazni.
A Vhr. 9. § új (2) bekezdését a 45/2001. (VI. 25.) FVM rendelet 2. §-a iktatta a szövegbe, egyidejűleg az eredeti (2)–(3) bekezdés számozását (3)–(4) bekezdésre változtatva. E módosító rendelet 12. § (1) bekezdése alapján a 9. § (2) bekezdését 2001. szeptember 1-jétől kell alkalmazni.
A Vhr. 9. § eredeti (2) bekezdésének számozását a 45/2001. (VI. 25.) FVM rendelet 2. §-a (3) bekezdésre változtatta.
A Vhr. 9. § eredeti (3) bekezdésének számozását a 45/2001. (VI. 25.) FVM rendelet 2. §-a (4) bekezdésre változtatta.
A Vhr. 11. §-a (4) bekezdésének b) pontja a 45/2001. (VI. 25.) FVM rendelet 3. §-ával megállapított szöveg.
A Vhr. 11. §-a (4) bekezdésének c) pontja a 45/2001. (VI. 25.) FVM rendelet 3. §-ával megállapított szöveg.
A Vhr. 19. §-a a 45/2001. (VI. 25.) FVM rendelet 4. §-ával megállapított szöveg.
A Vhr. 19. § (2) bekezdésének a) pontját a 45/2001. (VI. 25.) FVM rendelet 12. § (1) bekezdése alapján 2001. szeptember 1-jétől kell alkalmazni.
A Vhr. 26. § (4) bekezdése a) pontjának 3. alpontja a 45/2001. (VI. 25.) FVM rendelet 5. § (1) bekezdésével megállapított szöveg, e módosító rendelet 12. § (1) bekezdése alapján harmadik francia bekezdését 2001. szeptember 1-jétől kell alkalmazni.
A Vhr. 26. § (9) bekezdése a 45/2001. (VI. 25.) FVM rendelet 5. § (2) bekezdésével megállapított szöveg.
A Vhr. 41. § (1) bekezdése a 45/2001. (VI. 25.) FVM rendelet 6. §-ával megállapított szöveg.
A Vhr. 45/A. §-át a 45/2001. (VI. 25.) FVM rendelet 7. §-a iktatta a szövegbe.
A Vhr. 46. § (2) bekezdésének b) pontja a 45/2001. (VI. 25.) FVM rendelet 8. § (1) bekezdésével megállapított szöveg.
A Vhr. 46. § (2) bekezdésének d) pontja a 45/2001. (VI. 25.) FVM rendelet 8. § (2) bekezdésével megállapított szöveg.
A Magyar Közlöny 1996. évi 77. számában megjelent helyesbítésnek megfelelő szöveg.
A Vhr. 51. §-át a 45/2001. (VI. 25.) FVM rendelet 9. §-a iktatta a szövegbe.
Lásd a 86/1997. (XI. 26.) FM rendeletet.
Lásd a 26/1997. (IV. 18.) FM rendeletet.
A Vhr. 6. számú melléklete a 45/2001. (VI. 25.) FVM rendelet 10. §-ával megállapított szöveg.
A Vhr. 8. számú mellékletét a 45/2001. (VI. 25.) FVM rendelet 12. § (2) bekezdése hatályon kívül helyezte.
Az 1/1999. ( I. 14.) FVM rendelet 20. §-a (2) bekezdésének a) pontja szerint módosított szöveg.
Az 1/1999. ( I.14.) FVM rendelet 20. §-a (2) bekezdésének b) pontja szerint kiegészített szöveg.
A 12. számú melléklet második francia bekezdését az 1/1999. ( I. 14.) FVM rendelet 20. §-a (2) bekezdésének c) pontja iktatta a szövegbe.
A 13. számú melléklet 2. pontja az 1/1999. ( I. 14.)FVM rendelet 20. §-a (2) bekezdésének d) pontjával megállapított szöveg.
A 14. számú melléklet második francia bekezdését az 1/1999. ( I.14.) FVM rendelet 20. §-a (2) bekezdésének e) pontja iktatta a szövegbe.
A 15. számú melléklet ,,a kérelemhez mellékelni kell'' szövegrész utáni második francia bekezdését az 1/1999. ( I.14.) FVM rendelet 20. §-a (2) bekezdésének f) pontja iktatta a szövegbe.
A 16. számú melléklet ,,a kérelemhez mellékelni kell'' szövegrész utáni második francia bekezdését az 1/1999. ( I.14.) FVM rendelet 20. §-a (2) bekezdésének g) pontja iktatta a szövegbe.
A 17. számú melléklet második francia bekezdését az 1/1999. ( I. 14.) FVM rendelet 20. §-a (2) bekezdésének h) pontja iktatta a szövegbe.
A 18. számú melléklet 1.4. pontja az 1/1999. ( I. 14.) FVM rendelet 20. §-a (2) bekezdésének i) pontjával megállapított szöveg.
A 18. számú melléklet 1.9. pontját az 1/1999. ( I. 14.) FVM rendelet 20. §-a (2) bekezdésének j) pontja iktatta a szövegbe.
A 19. számú melléklet 1.2. pontja az 1/1999. ( I. 14.) FVM rendelet 20. §-a (2) bekezdésének k) pontjával megállapított szöveg.
A 22. számú melléklet a 45/2001. (VI. 25.) FVM rendelet 11. §-ának és 12. § (2) bekezdésének megfelelően módosított szöveg.
